Alotropia
Chamamos de Alotropia a capacidade de um único elemento químico formar duas ou mais substâncias simples diferentes. A palavra alotropia vem do grego allos, outro, e tropos, maneira e foi criada por Jöns Jacob Berzelius. Chamamos de alótropos as diferentes substâncias simples formadas. Os elementos capazes de formar alótropos são Oxigênio (O), Enxofre (S), Carbono (C) e Fósforo (P).
Oxigênio (O)
O oxigênio é encontrado na atmosfera em forma de gás oxigênio (O2) e em forma de gás ozônio (O3). A diferença entre eles é apenas a quantidade de átomos de oxigênio na molécula. Então podemos dizer as formas alotrópicas do elemento químico oxigênio são o gás oxigênio (O2) e o gás ozônio (O3). O gás oxigênio é indispensável para a vida da maioria dos seres vivos, além de ser essencial para a combustão de qualquer material. Já o gás ozônio é responsável pela formação da camada de ozônio, que fica de 20 a 40 km acima do planeta Terra. O ozônio tem a função de nos proteger dos raios ultravioletas, que são prejudiciais à saúde.
Enxofre (S)
O enxofre forma moléculas S8, que constituem o retículo cristalino molecular. Porém, ele tem duas formas diferentes, o enxofre rômbico e o enxofre monoclínico. Eles se diferem somente pela forma, que só é observada bem de perto. As duas formas têm cor amarelada.
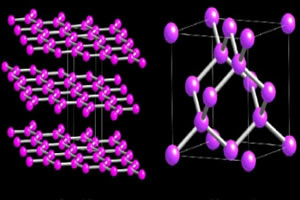
Moléculas de grafite e diamante
Carbono (C)
O elemento Carbono tem duas formas diferentes: o diamante e o grafite. A diferença entre eles é a organização dos átomos na molécula. O diamante é a substância natural mais dura que se conhece. Essa dureza se deve à maneira como os vários tetraedros de carbono se ligam.
Fósforo (P)
O elemento fósforo tem dois alótropos: o fósforo branco e o fósforo vermelho. A diferença entre eles é o número de átomos de fósforo na molécula.