Reações endotérmicas e exotérmicas
Existe uma área da Química chamada “Termoquímica” que estuda as reações químicas e também as mudanças de estado físico envolvendo trocar de energia na forma de calor. Basicamente, existem dois tipos de reação: as exotérmicas e as endotérmicas.
As reações exotérmicas são aquelas nas quais ocorre liberação de calor (o prefixo “exo” significa “para fora”). Já as reações endotérmicas são aquelas nas quais ocorre absorção de calor (o prefixo “endo” significa “para dentro”).
Reações Exotérmicas
Nas reações exotérmicas, o valor da entalpia (H) – ou o valor da energia global dos elementos (HP) – é sempre menor que a entalpia dos reagentes (HR). Assim, a variação da entalpia (ΔH) é sempre negativa.
A fórmula de uma reação exotérmica é:
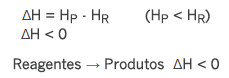
Fórmula de uma reação exotérmica
As reações exotérmicas podem ser representadas graficamente da seguinte forma:
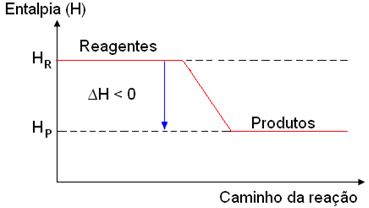
Gráfico de uma reação exotérmica
São exemplos de reações exotérmicas:
- Queima de um palito de fósforo;
- Combustão da gasolina ou do álcool;
- Queima do carvão;
- Queima de palha de aço;
- Queima de velas;
- Passagem do estado de vapor da água para o estado líquido (condensação);
- Formação da neve (solidificação da água);
- Bolsa de água quente;
- Queima dos alimentos que fornecem energia para o nosso organismo;
- Respiração.
Observando esses exemplos, podemos perceber que nas reações exotérmicas o sistema perde calor e o ambiente é aquecido.
Reações Endotérmicas
Por outro lado, nas reações endotérmicas, o valor da entalpia dos produtos (HP) é sempre maior que a entalpia dos reagentes (HR). Assim, a variação da entalpia (ΔH) é sempre positiva.
A fórmula de uma reação endotérmica é:
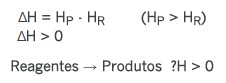
Fórmula de uma reação endotérmica
As reações endotérmicas podem ser representadas graficamente da seguinte forma:
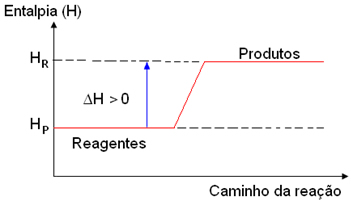
Gráfico de uma reação endotérmica
São exemplos de reações endotérmicas:
- Fotossíntese (as plantas absorvem a energia fornecida pelo sol);
- Fusão (para que o gelo derreta, ele precisa absorver calor do meio);
- Evaporação;
- Ebulição;
- Bolsa de gelo;
- Roupas secando no varal (a água evapora ao absorver a luz do sol);
- Gelo derretendo.
Observando esses exemplos, podemos perceber que nas reações endotérmicas o sistema ganha calor e o ambiente se resfria.