Química Orgânica
Convencionou-se chamar de química orgânica um ramo da química que trata dos compostos de carbono com propriedades químicas semelhantes. É importante ressaltar que nem todo composto que contenha carbono é orgânico (como exemplo, o dióxido de carbono), mas todos os compostos chamados orgânicos contém carbono.
No início dos estudos da química, acreditava-se que todos os compostos orgânicos eram originados de seres vivos, e que não poderiam ser sintetizados em laboratório. Por isso foi dado esse nome. Mas depois de mais estudos, foi verificada a possibilidade de sintetizar os compostos derivados do carbono.
Os compostos orgânicos existem em maior quantidade que os compostos inorgânicos. Isso se deve a uma das principais características do carbono, a tetravalência, ou seja, ele pode formar 4 ligações covalentes, formando assim uma infinidade de compostos.
Características do átomo de carbono
- É um átomo tetravalente, ou seja, forma sempre 4 ligações covalentes.
- É capaz de se ligar sequencialmente, formando cadeias.
- Suas ligações são equivalentes e podem ser formadas de diversas maneiras (simples, dupla e / ou tripla).
Classificação dos Carbonos
Um carbono pode ser classificado numa cadeia tomando como referência o número de carbonos diretamente ligados a ele. Veja o exemplo abaixo. O carbono (C) na cor amarela é um carbono quaternário, porque se liga a outros 4 carbonos; o carbono (C) na cor verde é um carbono terciário, pois se liga a outros 3 carbonos; o carbono (C) na cor azul é um carbono secundário, pois está ligados diretamente a outros dois carbonos; e o carbono (C) na cor vermelha, que está ligado a somente 1 carbono, é chamado de carbono primário.
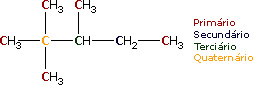
Veja uma cadeia e a classificação dos carbonos
- Carbono primário: está ligado a apenas 1 outro átomo de carbono.
- Carbono secundário: está ligado diretamente a no máximo a 2 outros carbonos.
- Carbono terciário: está ligado diretamente a até 3 outros átomos de carbono.
- Carbono quaternário: está ligado diretamente a 4 átomos de carbono.
As cadeias orgânicas também podem ser classificadas, dependendo de suas características. Podem ser cíclicas (fechadas) ou acíclicas (abertas), saturadas ou insaturadas, homogêneas ou heterogêneas.
Veja aqui as classificações de cadeias orgânicas.
Funções Orgânicas
Os compostos orgânicos também se dividem de acordo com o seu comportamento químico e presença de agrupamentos de átomos em suas estruturas. Chamamos essas divisões de funções orgânicas. São elas:
Hidrocarbonetos
São compostos constituídos por átomos de carbono e hidrogênio, apenas. Sendo essa função composta por uma ampla gama de combustíveis. Exemplos: metano, propano, acetileno.
Álcoois
Os alcoóis são constituídos por radicais de hidrocarbonetos (carbono e hidrogênio) ligados a uma ou mais hidroxilas (moléculas de água que perderam um átomo de hidrogênio). Entretanto, nunca podem ser considerados bases de Arrhenius (pois não liberam essa hidroxila em meio aquoso).
Fenóis
São cadeias aromáticas (hidrocarbonetos) ligados a uma ou mais hidroxilas. Diferindo-se dos alcoóis, portanto, por apresentarem estrutura em anéis rodeados por grupos OH.
Éteres
Essas funções são compostas por um átomo de oxigênio entre duas cadeias carbônicas. Sendo estas cadeias também de hidrocarbonetos (radicais alquila ou arila).
Ésteres
São bem parecidas com os éteres, pois também possuem átomos de oxigênio entre as cadeias carbônicas (radicais). Porém, diferem-se destes por possuírem um grupo carbonilo (CO) também entre os carbonos. Assim, a molécula é estruturada por: radical – carbonilo – oxigênio – radical.
Aldeídos
São formados por um radical orgânico (alifático ou aromático) ligado a um ou mais grupos formilo (HCO).
Cetonas
As cetonas são compostas por dois radicais orgânicos (alifáticos ou aromáticos) ligados entre si pelo grupo carbonilo (CO). É a essa função que pertence a acetona comercial (propanona – CH3COCH3).
Ácidos Carboxílicos
São radicais alquila, alquenila, arila ou hidrogênio ligados a pelo menos um grupo carboxílico (COOH). E, geralmente, são ácidos fracos (liberam poucos íons H+ em meio aquoso).