Isótopos
Em 1914 o físico inglês Frederick Soddy descobriu que um mesmo elemento químico pode apresentar-se com pesos atômicos diferentes, e denominou essas variações de “isótopos”. O termo é uma combinação de duas palavras gregas (iso e topos) que significam “o mesmo lugar”, porque os isótopos, embora apresentem massas atômicas diferentes, ocupam o mesmo lugar na Tabela Periódica dos Elementos. Ocorre que o núcleo de seus átomos diferencia-se unicamente pela quantidade de nêutrons, o que os faz ser identificados por seus pesos atômicos. Os isótopos de urânio U235 e U238, por exemplo, do ponto de vista químico são o mesmo elemento Urânio, isto é, possuem as mesmas propriedades químicas. Diferenciam-se pelas propriedades físicas, inclusive a massa atômica que é respectivamente 235 e 238.
Os isótopos podem apresentar outras diferenças nas propriedades físicas, como se verifica em laboratório pela facilidade com que um campo magnético os desvia de sua trajetória, ou pela maior ou menos dificuldade que encontram em atravessar algumas membranas muito finas.
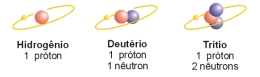
Isótopos do Hidrogênio
A Utilização dos Isótopos
Embora a maioria dos isótopos naturais seja estável, alguns são radiativos. Mas, em reatores nucleares é possível produzir-se instáveis artificialmente. Esses isótopos artificiais são chamados de “radioisótopos” e têm amplo campo de aplicação. Fábricas de instrumentos de precisão empregam-nos para descobrir minúsculas imperfeições no metal fundido e para conseguir medidas extremamente delicadas. Na medicina, os isótopos de cobalto e rádio são usados no tratamento do câncer, enquanto o de iodo é empregado para examinar as glândulas tireoides de pacientes em chapas de raios X ou fluoroscópios. Na agricultura, frequentemente são utilizados radioisótopos para estudar o comportamento das plantas quando recebem fertilizantes.